孕前持续抗病毒治疗预防乙型肝炎病毒围产期传播的有效性和安全性
摘要
很少进行研究来评估从孕前开始进行连续抗病毒治疗的安全性和有效性。在本研究中,招募了136例患有慢性HBV感染的合格妇女,并分配给活动性慢性乙型肝炎(CHB)(A,B或C组)或慢性HBV携带者(D组)。在孕前(A组),妊娠早期(B组)或妊娠晚期(C组和D组)进行抗病毒治疗。对所有婴儿进行免疫预防。在分娩时和产后7个月评估母亲的HBV状态和ALT。在7个月大时检查后代的HBV状况。A组妇女在整个怀孕期间均表现出较低的HBV DNA水平和正常的ALT。所有分娩的妇女的HBV DNA水平均低于10 6 IU / ml,但A组中HBV DNA水平较低的患者比例高于其他三组(P <0.05)。四组之间的产科并发症无差异。完成随访的婴儿中,没有一个在7个月大时出现HBsAg阳性。在研究队列中,先天性畸形和婴儿生长指标相似。从怀孕前到整个怀孕期间持续进行抗病毒治疗对于活跃的CHB母亲及其婴儿都是有效和安全的。
介绍
慢性HBV感染是肝硬化和肝细胞癌(HCC)的主要原因,在全世界,尤其是在亚洲和非洲1,仍然是重要的公共卫生问题。大约3.6%的全球人口通过围产期传播(这是HBV的主要传播途径)2长期感染HBV 。每年大约有200万儿童通过母婴传播(MTCT)3感染HBV 。不幸的是,这些儿童中有90%成为慢性HBV感染,可能在数年或数十年之内发展为进行性肝纤维化,肝硬化,甚至HCC 4。因此,阻断MTCT是降低总体HBV患病率和健康负担的重要措施。
乙肝疫苗和乙肝免疫球蛋白(HBIG)的联合免疫通常用于预防HBV 4的 MTCT 。然而,免疫预防失败婴儿的约2-10%5,6,其母亲是乙型肝炎e抗原(HBeAg)阳性或高病毒血症7,8。故障率甚至可以提高至30%为出生以高HBV DNA水平(HBV DNA≥10母亲的婴儿6 IU / ml)的9,10,11。因此,控制孕妇HBV DNA水平是预防HBV MTCT的关键措施。对于HBV DNA水平高的母亲,请使用替比夫定(LDT)12或富马酸替诺福韦酯(TDF)13早期或晚期妊娠抑制病毒复制过程中,在具有免疫预防组合,被认为是对减少HBV母婴传播的重要途径12,13,14。但是,某些在妊娠中期或晚期接受抗病毒治疗的母亲所生的婴儿感染了HBV 15,这表明抗病毒药物的预防应更早开始。但是,开始抗病毒治疗的最佳或最佳时间仍然不确定。
有些育龄妇女活动性慢性乙型肝炎(CHB)应采取口服抗病毒药物在孕前,因为慢性HBV感染者的抗病毒治疗可以控制肝炎暴发,减少肝硬化,肝癌和死亡的发生率16,17。这些患者必须长期服用口服抗病毒药,甚至终身服用,因为口服抗病毒药只能抑制HBV而不是杀死HBV。然而,肝炎耀斑和病毒学复发的抗病毒治疗的不连续之后是常见的18,19。因此,长期治疗对于维持病毒学应答是必不可少的。此外,HBV可以通过生殖细胞20垂直传播到后代。目前尚不清楚,如果孕妇在怀孕前肝酶恢复正常,是否应在整个妊娠期间继续服用抗病毒药物。迄今为止,抗病毒治疗通常是在育龄妇女怀孕后开始的。在胚胎植入阶段很少进行有关抗病毒治疗的临床研究。在本研究中,我们评估了从受孕前到整个妊娠期间开始的连续抗病毒治疗对于降低HBV的MTCT是否安全有效。
结果
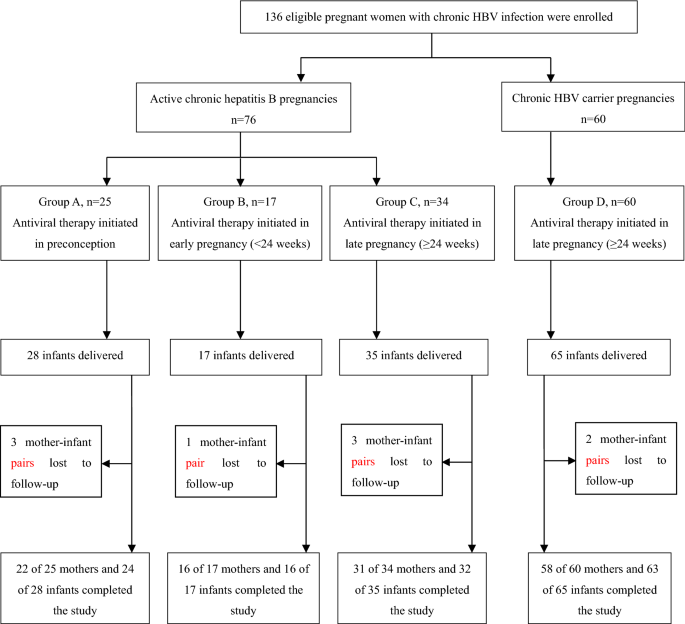
从2017年1月1日到2018年12月31日,共筛查了164名孕妇。然后,共有136名合格孕妇入组,并分为活跃的慢性乙型肝炎(CHB)组(即A,B或C组)或慢性HBV携带者组(D组)。抗病毒治疗分别在受孕前(A组25例),妊娠早期(B组17例)或妊娠晚期(C组34例和D组60例)进行(图 1)。最后,我们获得了这四个研究组的成功随访率为85.7–96.9%。
母亲抗病毒治疗的疗效和安全性
如表1所示,这些组之间的孕产妇年龄无统计学差异。在每个组中,大多数入组病例的乙型肝炎e抗原(HBeAg)均为阳性。A组患者在孕前表现出较低的HBV DNA水平和ALT正常,这是由于在孕前开始抗病毒治疗以及整个孕期连续使用抗病毒药物。分娩时,A组中HBV DNA水平低的患者比例高于其他三组(P <0.05)。此外,四个研究组中的所有孕妇的HBV DNA水平均低于10 6 交货时IU / ml。B组17例患者中有3例(17.6%),C组34例中有10例(29.4%)和D组60例中有4例(6.7%)在分娩时出现ALT异常,但所有A组患者在分娩时ALT均正常。
四组之间的分娩方式和胎龄均无统计学差异(表2)。在四个研究组中,选定的妊娠并发症在统计学上也没有统计学差异(P > 0.05)。
胎儿和婴儿抗病毒治疗的安全性
如表3所示,四组的胎儿发育指标和婴儿生长无统计学差异(P > 0.05)。四组之间的出生体重,体长和Apgar评分在1分钟时相似(P > 0.05)。新生儿并发症包括先天性畸形,早产和胎儿/新生儿死亡率没有统计学上的显着差异(P > 0.05)。在四组中,婴儿的体重,身长,6个月大时的异常发育没有统计学差异(P > 0.05)。
抗病毒治疗对HBV MTCT的有效性
四个随访组的HBV MTCT率见表4。接受随访的婴儿均未发现乙肝表面抗原(HBsAg)阳性,而所有婴儿均显示出乙肝表面抗体(HBsAb)阳性。B组肝炎病毒B核心抗原(HBcAb)抗体阳性率最高,D组最低(P <0.05)。在三个活跃的CHB组中,A组的HBcAb阳性率最低。
讨论区
在本研究中,我们发现A组患者在整个怀孕期间均表现出较低的HBV DNA水平和正常的ALT。A组中HBV DNA水平较低的患者比例高于其他三组(P <0.05)。分娩时,A组所有患者的ALT均正常,而其他三组中的一些患者的ALT均异常。与妊娠后期服用抗病毒药物的患者(C组和D组)相比,孕前或妊娠早期服用抗病毒药物的患者(A组和B组)在产科并发症方面没有差异。此外,他们的先天畸形和新生儿生长指标在四组中相似。它已经证实,在怀孕的第二个和第三个三个月开始抗病毒治疗是有效的预防HBV的母婴传播12,13,14。不幸的是,母亲所生婴儿的一些第二或孕晚期感染了乙肝病毒在接受抗病毒治疗13,15。结果,开始抗病毒治疗的最有效时间未知。我们的结果表明,对于患有活动性慢性乙型肝炎(CHB)的孕妇,从孕前到整个妊娠期间持续进行抗病毒治疗对母亲和婴儿都是安全的,并且是减少进入子孙体内HBV的有效手段。
在我们的研究中,我们关注活跃的CHB患者和高HBV DNA水平的慢性HBV携带者,因为他们都应接受抗病毒治疗,以控制肝炎发作并降低HBV的MTCT。与C组或D组(妊娠晚期进行抗病毒治疗)相比,其他两组(A组,先孕后的抗病毒治疗; B组,孕早期的抗病毒治疗)没有出现明显的母婴并发症(P > 0.05)。我们的结果表明,从孕前到整个怀孕期间,对母亲及其后代采取TDF / LDT治疗可能是安全的。尽管我们的研究样本量相对较小,但那些孕妇具有可比的特征(例如年龄差异小和独特的中国种族),并且在整个研究过程中我们使用了一致的实验室测试方法。在未来的研究中,可能需要更多的孕妇来确定抗病毒药物对先天性异常或先天缺陷是否可能有影响。此外,由于以下起坐只能是28-36周内进行产后在以往的研究13,21,22,我们对安全性的评估可能不完整,因此需要延长随访时间。
从妊娠前一直持续进行抗病毒治疗,尽管整个妊娠对活跃的CHB患者保持肝功能正常并控制母体肝损害非常重要23。停止抗病毒治疗可能导致CHB患者严重加重甚至肝功能衰竭24。与非孕妇相比,孕妇更容易因慢性HBV感染而导致肝衰竭,因为HBV感染是中国妊娠期间严重肝炎的最重要原因25。ALT水平和HBV DNA的负荷水平可以在整个妊娠期间被增强,这是因为改变的免疫调节可能怀孕期间有助于HBV复制和ALT水平的提高26,27,28。此外,HBV和ALT耀斑在怀孕期间甚至可能很严重29。如果ALT反复发作且严重,则CHB患者容易发展为肝纤维化,甚至肝硬化30。结果,一些患有CHB的孕妇在怀孕期间可能发展为严重的肝纤维化,肝硬化。在我们的研究A组(妊娠前的抗病毒治疗)中,整个妊娠期间出现ALT正常的患者可能是由于妊娠前开始抗病毒治疗以及整个妊娠期间继续接受该方案。在我们的B组和C组中,这些患者的肝功能在接受抗病毒治疗后逐渐恢复正常。没有患者发展为肝功能衰竭或肝硬化。但是,B组的一名患者和C组的一名患者均因自己撤药而被排除在外。两名患者在服用抗病毒药物时显示ALT正常。停用抗病毒药物后的ALT分别为544 U /升和422.2 U /升。然而,
从受孕前开始进行持续的抗病毒治疗似乎是控制母体肝损害并减少HBV从母亲向胎儿传播的有效手段。与分娩时其他组的孕妇HBV DNA水平和ALT水平相比(表1),A组患者(妊娠前进行抗病毒治疗)在整个妊娠期间均具有较低的HBV DNA水平和ALT正常,这表明从妊娠前至整个妊娠期间连续进行抗病毒治疗有效降低了孕妇的HBV DNA水平和肝损害。孕妇的HBV DNA水平越低,HBV进入后代体内的风险就越低。乙肝病毒进入后代体内的风险越低,婴儿免疫预防的成功率就越高。此外,在本研究中,未完成随访的所有婴儿均未显示HBsAg阳性,所有婴儿均显示HBsAb阳性。在我们的研究中,没有婴儿被乙肝病毒感染。它通常接受的是母体HBV DNA水平在HBV的母婴传播起着至关重要的作用4,9,10,11。最近的几项研究 13,14,21报道,HBV母婴传播率下降,如果病人在妊娠后期采取抗病毒治疗(例如,林,LDT和TDF)。我们的研究结果还表明,妊娠期抗病毒治疗降低了HBV的MTCT发生率。而且,在我们的研究中,一些HBcAb阳性,HBsAb阳性和HBsAg阴性的婴儿表明,即使未发生HBV的MTCT,HBV仍会进入一些后代体内。因为在0-24个月年龄大三阳阳性率可能部分来自母亲的被动转移造成的身体或等于说HBV曾经进入婴儿体内 31,32,我们将进一步研究HBcAb对婴儿的意义。
在以前的研究中13,22,抗病毒治疗持续产后1个月到乙肝病毒母婴传播的中断。在我们的研究中,怀孕期间HBV DNA水平高且肝功能正常的患者在分娩后立即停止抗病毒治疗。然后这些母亲可以母乳喂养婴儿。尽管EASL在2017 年的指南19中建议应建议在产后继续进行TDF治疗的患者进行母乳喂养,但大多数母亲在分娩后继续进行TDF治疗的母亲仍然不愿母乳喂养,因为他们担心TDF对婴儿可能有任何不利影响在我们的临床实践中。此外,TDF药物标签是中国肝病学会的临床指南33,并且《亚太地区34》的临床指南并未明确建议在母亲接受TDF治疗时应鼓励母乳喂养。
总而言之,我们的研究结果表明,从妊娠前到整个妊娠期间持续进行抗病毒治疗对于活跃的CHB母亲及其婴儿都是安全的。这种有效的方法可以减少进入子孙体内的HBV。整个怀孕期间持续进行抗病毒治疗可以预防HBV的MTCT。此外,抗病毒疗法似乎可以控制妊娠期肝炎发作并促进ALT正常化。对于有活动性CHB的准孕妇,开始抗病毒治疗可能会提前进入孕前。
方法
耐心
当前的前瞻性队列研究已获得广州医科大学第三附属医院的机构伦理审查委员会的批准,并且是根据1964年《赫尔辛基宣言》及其后续修正案中规定的伦理标准进行的。在本研究中,每位患者均获得知情的书面同意。本研究已在ClinicalTrials.gov(No. NCT03181607)中注册。我们可以访问研究数据,并已审核并批准了最终稿件。
这项多中心队列研究于2017年1月至2018年12月进行。自愿参加了在中国六家医院就诊且符合以下纳入标准和排除标准的慢性HBV感染孕妇。纳入标准如下:(a)HBV感染史≥6个月;(b)HBsAg阳性;(c)对于在孕前期已接受抗病毒治疗的患者,不能停止治疗;对于从未接受过抗病毒治疗的患者,ALT≥正常上限(ULN)的2倍,或HBV DNA水平≥10 4 IU / ml(HBeAg阳性)或HBV DNA水平≥10 3 IU / ml(HBeAg阴性),传统的保护肝脏和还原酶治疗失败;(四)患者依从性良好。
排除标准如下:(a)具有抗HIV,HCV,HDV或其他形式的慢性肝病抗体的患者;(b)肝细胞癌,失代偿性肝病,自身免疫性肝炎或严重的肾脏,心血管,呼吸或神经系统合并症的证据;(c)与肾毒性药物,糖皮质激素,细胞毒性药物,非甾体类抗炎药或免疫调节剂同时治疗;(d)胎儿畸形,胎儿发育异常或胎盘异常的超声检查证据;(e)流产先兆的临床体征;(f)有复杂妊娠史;(g)自行停药。
学习规划
如图1所示 根据纳入标准和排除标准,我们纳入了136名合格的慢性HBV感染孕妇。他们被分为以下四组。在A组中,患有活动性CHB的患者由于肝脏功能异常,每天一次口服300毫克富马酸替诺福韦酯(TDF,葛兰素史克(GlaxoSmithKline))或600毫克替比夫定(LDT,诺华中国)。当他们的肝酶在怀孕前恢复正常时,他们在整个怀孕期间连续服用TDF或LDT。在B组和C组中,CHB孕妇分别在怀孕早期(少于24个孕周)和妊娠晚期(超过24个孕周)显示肝功能异常。然后他们开始分别每天服用TDF(300毫克/次)或LDT(600毫克/次)。在D组中6 IU / ml)和正常肝功能。为了降低HBV DNA水平和MTCT的风险,在妊娠晚期,用TDF(口服300毫克/次,Qd)或LDT(口服600毫克/次,Qd)对其进行治疗。
在怀孕期间,所有患者每4周进行一次随访,以监测不良事件和实验室检查结果(肝功能检查,HBV DNA水平,血液学检查等)。分娩后,A,B和C组的患者继续接受TDF / LDT治疗,D组的患者停止接受TDF / LDT治疗。所有这些患者在分娩的前三个月中每4周进行一次随访。随后,他们分别在产后第24周和第28周接受了随访。
所有婴儿均接受100 IU乙型肝炎免疫球蛋白(HBIG,华兰生物技术有限公司,中国河南省新乡市)和10μg重组乙型肝炎疫苗(RHBV,深圳康泰生物技术有限公司,深圳)出生后1至24小时内进行肌肉注射。在4周龄时给予相同剂量的HBIG。在第4周和第24周给予相同剂量的重组乙型肝炎疫苗。
所有母亲及其婴儿均在产后7个月内接受了随访。
结果指标
主要结果包括母亲抗病毒治疗的有效性和安全性。我们分析了分娩时和产后7个月的孕妇HBV DNA水平和丙氨酸转氨酶(ALT)。为了衡量抗病毒治疗对母亲的安全性,分析了母亲的不良并发症。
次要结果包括阻断HBV MTCT的有效性以及TDF / LDT对后代的安全性。评估胎儿发育指标,如出生体重,身长和出生时及6个月大时的先天性异常,以评估抗病毒治疗对胎儿并发症的安全性。在7个月大时测定婴儿的HBV抗原和抗体状态,以评估阻断HBV MTCT的有效性。
统计分析
使用SPSS v22.00统计分析软件(SPSS Inc,芝加哥,伊利诺伊州)分析所有数据。描述性变量表示为平均值±标准偏差(SD)或百分比。方差分析(ANOVA)检验和χ2检验分别用于比较定量变量和分类变量。在P值<0.05时,差异被认为具有统计学意义。
结论
我们从该临床试验中获得的发现显然支持了我们的假设,即从妊娠前到整个妊娠期间持续进行抗病毒治疗对于活跃的CHB母亲及其婴儿是安全的。抗病毒疗法似乎可以控制妊娠期肝炎发作并促进ALT正常化。对于有活动性CHB的准孕妇,开始抗病毒治疗可能会提前进入孕前。
|
|